الثلاثاء 17 سبتمبر 2013. - حدد علماء من معهد شنغهاي للمسائل الطبية ومعهد أبحاث سكريبس بأكبر قدر ممكن من الدقة القفل المفضل لفيروس العوز المناعي البشري لدخول خلايا الجهاز المناعي لجسم الإنسان. وهو مصحح ، CCR5 ، والذي يوجد على سطح الخلايا المدافعة أو الخلايا اللمفاوية. ليس هذا هو السبيل الوحيد لدخول فيروس نقص المناعة البشرية ، بل هو الطريق الأكثر أهمية.
يحتاج فيروس العوز المناعي البشري (HIV) إلى مستقبلات CD4 لإصابة الخلايا اللمفاوية المختلفة في الكائن الحي ، ولكن يجب أيضًا أن تتفاعل مع واحد من المستقبلين المشتركين الموجودين أيضًا على سطح الخلية: CCR5 أو CXCR4. تمكن الباحثون الصينيون والأميركيون من تكوين صورة مثالية لأول صورة ، مضيفين ذلك إلى ما قاموا به بالفعل من جهة أخرى.
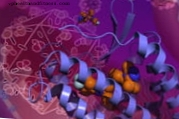
إن الصورة المثالية ليست أكثر من بنية ذرية عالية الدقة للمُصوِّت ، ما يسمى بلورة ، وهو أمر ، وفقًا لمدير منطقة علم الأمراض الجزيئية بالمركز الوطني للميكروبيولوجيا ، خوسيه الكامي ، يصعب تحقيقه في هذا النوع من الجزيئات ، والذي يبرر نشر هذه النتيجة في مجلة العلوم المرموقة.
كما أوضح هذا الخبير ، في بداية الإصابة ، يستخدم 100٪ من فيروس نقص المناعة البشرية مصحح CCR5 لدخول الخلية ، لكن في حوالي 40٪ من المرضى ، تتغير الفيروسات لاستخدام الأخرى مصحح ، CXCR4. في ذلك الوقت ، تغير الفيروسات اسمها الأخير وتنتقل من يطلق عليها "من المدارية R5" إلى الفيروسات "من المدارية X4". لزيادة تعقيد المعادلة ، تدخل بعض الفيروسات - المدارات R5X4 - في وقت واحد من خلال الموقعين.
يقول الكامى: "إنه باب ذو قفلين ؛ لذلك ، عندما يتم حظر أحدهما بدواء ، يمكن للفيروس فتح الباب باستخدام القفل الآخر". لم يتم تحقيق هذه الكتلة الدوائية إلا مرة واحدة فقط على CCR5 بفضل Maraviroc ، وهو دواء يستخدم اليوم في المصل المصل عندما تتوقف بعض التوليفات الموضحة في السطر الأول من العلاج.
إن أهم نتيجة للنتائج المنشورة في "العلوم" هي أنه من خلال البنية البلورية لـ CCR5 ، يمكن تصميم عقاقير جديدة تعمل على هذا الهدف ، وبالتالي تمنع دخول فيروس نقص المناعة البشرية من خلال هذا المستقبل المساعد. تتأثر هذه الفكرة بالتحديد بالافتتاح الذي يرافق المقال ، الذي كتبه الباحث في جامعة كورنيل بير يوهان كلاسي. يشير المؤلف إلى أنه لن يعمل فقط على تصنيع أدوية جديدة ضد CCR5 ، ولكن أيضًا لتحسين المعرفة حول تفاعل الفيروس مع أجزاء أخرى من الخلايا ، مثل المظروف.
يقول الكامي: "يمكن تصميم الأدوية أولاً على الكمبيوتر ثم بطريقة حقيقية تتناسب تمامًا مع البنية المحددة حديثًا". ولكن ، بالإضافة إلى ذلك ، يمكن أن يؤدي هذا الاكتشاف افتراضيًا إلى تحسن كبير في نوعية حياة المرضى الذين يعانون من المصل. وقال الكامي "في الوقت الحالي ، لدينا بالفعل إمكانية السيطرة على الفيروس بحبوب يومية واحدة ، لكن في المستقبل ، يمكنك التفكير في علاج سيُدار مرتين أو حتى مرة واحدة في الأسبوع".
تتم إضافة بلورة هذا المستقبِل المشترك إلى بلورات أخرى من أجزاء أخرى من الفيروس ، مثل غلافه أو غلافه أو البروتياز. كل هذه الهياكل أدت إلى تطوير عقاقير جديدة ضد فيروس نقص المناعة البشرية ، ويمكن القول إنها ساهمت في حقيقة أن الفيروس قد انتقل من كونه قاتلاً في معظم الحالات إلى السيطرة عليه بالأدوية.
ميزة أخرى من الاكتشاف هي أنه "سيساعد على فهم سبب وجود فيروسات تفضل قفلًا أو آخر لفتح باب المدخل" ، كما يشرح اختصاصي CNM.
كان مؤلفو الدراسة يحاولون صنع هذه الصورة الجزيئية لمدة ست سنوات ، حيث اختار المؤلف الرئيسي بيلي وو ، من Materia Medica ، معهد سكريبس للأبحاث للقيام بتدريبات ما بعد الدكتوراه في متلقي فيروس نقص المناعة البشرية ، حيث تدرب في مختبر ريموند ستيفنز. ، وآخر من المؤلفين. وقال الأخير في بيان صحفي "الآن بعد أن أصبح لدينا الهياكل ثلاثية الأبعاد لكلا مستقبلين ، فمن المحتمل جدًا أن نرى الجيل الجديد من العلاجات ضد فيروس نقص المناعة البشرية".
لتحقيق هذه الصورة عالية الجودة ، استخدم العلماء على وجه التحديد الدواء الذي يحظر مدخل المصحح ، لأنه "يستقر CCR5 في موقف واحد" ، يوضح Alcami.
الباحث الإسباني على دراية بعمل زملائه الصينيين والأمريكيين. في الواقع ، في دراسة "العلوم" ، تم الإشارة إلى عملين شارك في تأليفه مع عالم إسباني آخر ، خافيير غارسيا بيريز وباحثين من معهد باستور. في واحد منهم حددوا ، دون الحصول على "رسم" الكريستال ، والتفاعلات بين Maraceroc والمصحح الذي يعمل عليه. في الجانب الآخر ، تمت دراسة بعض جوانب مقاومة العقاقير ، وعلى وجه التحديد فائدة أخرى محتملة لهذا الاكتشاف ، والتي سوف تعمل أيضًا على البدء في فهم سبب توقف مثل هذا الدواء الفعال في بعض الحالات.
يقول الكامي إن هناك حاليا 26 عقارًا ضد فيروس نقص المناعة البشرية. يقول: "على الرغم من أنه يمكن استبعاد 10 أو 12 لأنها أصبحت قديمة ، لا يزال أمامنا 14 عامًا. الأولوية ليست الحصول على عدد أكبر من الأدوية ، ولكن قبل كل شيء الجزيئات التي تعمل على أهداف جديدة في دورة الفيروسات".
على الرغم من أن Maraviroc هو دواء من ما يسمى السطر الثاني (لم يتم وصفه للمريض الذي تم تشخيصه حديثًا بفيروس نقص المناعة البشرية) ، إلا أن هذا الدواء مهم جدًا لأنه الدواء الوحيد الذي يتم تسويقه حاليًا ويمنع دخول الفيروس إلى الخلية. ليس من المفترض أن تتدخل في القضاء على الفيروس.
يقول: "إنه دواء قوي ، قليل السمية وعمر طويل للغاية ، وهو ما يسمح بالحلم بمزيج علاجي مستقبلي لا يجب تناوله يوميًا".
في عالم مثالي ، يمكن أن يتكون هذا المزيج المحتمل من مزيج من عقارين من شأنه أن يغلق مرور فيروس نقص المناعة البشرية في المستقبلين المشاركين. لأول مرة ، Maraviroc موجود بالفعل ، على الرغم من أن هذه البلورة ستسمح على الأرجح بتطوير عقاقير جديدة تهدف إلى منع استخدام مصحح CCR5 بواسطة فيروس نقص المناعة البشرية. بالنسبة لمستقبلات CXCR4 المشتركة ، لم يكن من الممكن توليد أي دواء ، على الرغم من أن البلورة تم نشرها لمدة ثلاث سنوات. "فشلت جميع المحاولات بسبب سمية" ، يخلص Alcami.
المصدر:
علامات:
الصحة جنس الأدوية
يحتاج فيروس العوز المناعي البشري (HIV) إلى مستقبلات CD4 لإصابة الخلايا اللمفاوية المختلفة في الكائن الحي ، ولكن يجب أيضًا أن تتفاعل مع واحد من المستقبلين المشتركين الموجودين أيضًا على سطح الخلية: CCR5 أو CXCR4. تمكن الباحثون الصينيون والأميركيون من تكوين صورة مثالية لأول صورة ، مضيفين ذلك إلى ما قاموا به بالفعل من جهة أخرى.
إن الصورة المثالية ليست أكثر من بنية ذرية عالية الدقة للمُصوِّت ، ما يسمى بلورة ، وهو أمر ، وفقًا لمدير منطقة علم الأمراض الجزيئية بالمركز الوطني للميكروبيولوجيا ، خوسيه الكامي ، يصعب تحقيقه في هذا النوع من الجزيئات ، والذي يبرر نشر هذه النتيجة في مجلة العلوم المرموقة.
كما أوضح هذا الخبير ، في بداية الإصابة ، يستخدم 100٪ من فيروس نقص المناعة البشرية مصحح CCR5 لدخول الخلية ، لكن في حوالي 40٪ من المرضى ، تتغير الفيروسات لاستخدام الأخرى مصحح ، CXCR4. في ذلك الوقت ، تغير الفيروسات اسمها الأخير وتنتقل من يطلق عليها "من المدارية R5" إلى الفيروسات "من المدارية X4". لزيادة تعقيد المعادلة ، تدخل بعض الفيروسات - المدارات R5X4 - في وقت واحد من خلال الموقعين.
يقول الكامى: "إنه باب ذو قفلين ؛ لذلك ، عندما يتم حظر أحدهما بدواء ، يمكن للفيروس فتح الباب باستخدام القفل الآخر". لم يتم تحقيق هذه الكتلة الدوائية إلا مرة واحدة فقط على CCR5 بفضل Maraviroc ، وهو دواء يستخدم اليوم في المصل المصل عندما تتوقف بعض التوليفات الموضحة في السطر الأول من العلاج.
الآثار العملية
إن أهم نتيجة للنتائج المنشورة في "العلوم" هي أنه من خلال البنية البلورية لـ CCR5 ، يمكن تصميم عقاقير جديدة تعمل على هذا الهدف ، وبالتالي تمنع دخول فيروس نقص المناعة البشرية من خلال هذا المستقبل المساعد. تتأثر هذه الفكرة بالتحديد بالافتتاح الذي يرافق المقال ، الذي كتبه الباحث في جامعة كورنيل بير يوهان كلاسي. يشير المؤلف إلى أنه لن يعمل فقط على تصنيع أدوية جديدة ضد CCR5 ، ولكن أيضًا لتحسين المعرفة حول تفاعل الفيروس مع أجزاء أخرى من الخلايا ، مثل المظروف.
يقول الكامي: "يمكن تصميم الأدوية أولاً على الكمبيوتر ثم بطريقة حقيقية تتناسب تمامًا مع البنية المحددة حديثًا". ولكن ، بالإضافة إلى ذلك ، يمكن أن يؤدي هذا الاكتشاف افتراضيًا إلى تحسن كبير في نوعية حياة المرضى الذين يعانون من المصل. وقال الكامي "في الوقت الحالي ، لدينا بالفعل إمكانية السيطرة على الفيروس بحبوب يومية واحدة ، لكن في المستقبل ، يمكنك التفكير في علاج سيُدار مرتين أو حتى مرة واحدة في الأسبوع".
تتم إضافة بلورة هذا المستقبِل المشترك إلى بلورات أخرى من أجزاء أخرى من الفيروس ، مثل غلافه أو غلافه أو البروتياز. كل هذه الهياكل أدت إلى تطوير عقاقير جديدة ضد فيروس نقص المناعة البشرية ، ويمكن القول إنها ساهمت في حقيقة أن الفيروس قد انتقل من كونه قاتلاً في معظم الحالات إلى السيطرة عليه بالأدوية.
ميزة أخرى من الاكتشاف هي أنه "سيساعد على فهم سبب وجود فيروسات تفضل قفلًا أو آخر لفتح باب المدخل" ، كما يشرح اختصاصي CNM.
كان مؤلفو الدراسة يحاولون صنع هذه الصورة الجزيئية لمدة ست سنوات ، حيث اختار المؤلف الرئيسي بيلي وو ، من Materia Medica ، معهد سكريبس للأبحاث للقيام بتدريبات ما بعد الدكتوراه في متلقي فيروس نقص المناعة البشرية ، حيث تدرب في مختبر ريموند ستيفنز. ، وآخر من المؤلفين. وقال الأخير في بيان صحفي "الآن بعد أن أصبح لدينا الهياكل ثلاثية الأبعاد لكلا مستقبلين ، فمن المحتمل جدًا أن نرى الجيل الجديد من العلاجات ضد فيروس نقص المناعة البشرية".
لتحقيق هذه الصورة عالية الجودة ، استخدم العلماء على وجه التحديد الدواء الذي يحظر مدخل المصحح ، لأنه "يستقر CCR5 في موقف واحد" ، يوضح Alcami.
الباحث الإسباني على دراية بعمل زملائه الصينيين والأمريكيين. في الواقع ، في دراسة "العلوم" ، تم الإشارة إلى عملين شارك في تأليفه مع عالم إسباني آخر ، خافيير غارسيا بيريز وباحثين من معهد باستور. في واحد منهم حددوا ، دون الحصول على "رسم" الكريستال ، والتفاعلات بين Maraceroc والمصحح الذي يعمل عليه. في الجانب الآخر ، تمت دراسة بعض جوانب مقاومة العقاقير ، وعلى وجه التحديد فائدة أخرى محتملة لهذا الاكتشاف ، والتي سوف تعمل أيضًا على البدء في فهم سبب توقف مثل هذا الدواء الفعال في بعض الحالات.
يقول الكامي إن هناك حاليا 26 عقارًا ضد فيروس نقص المناعة البشرية. يقول: "على الرغم من أنه يمكن استبعاد 10 أو 12 لأنها أصبحت قديمة ، لا يزال أمامنا 14 عامًا. الأولوية ليست الحصول على عدد أكبر من الأدوية ، ولكن قبل كل شيء الجزيئات التي تعمل على أهداف جديدة في دورة الفيروسات".
على الرغم من أن Maraviroc هو دواء من ما يسمى السطر الثاني (لم يتم وصفه للمريض الذي تم تشخيصه حديثًا بفيروس نقص المناعة البشرية) ، إلا أن هذا الدواء مهم جدًا لأنه الدواء الوحيد الذي يتم تسويقه حاليًا ويمنع دخول الفيروس إلى الخلية. ليس من المفترض أن تتدخل في القضاء على الفيروس.
يقول: "إنه دواء قوي ، قليل السمية وعمر طويل للغاية ، وهو ما يسمح بالحلم بمزيج علاجي مستقبلي لا يجب تناوله يوميًا".
في عالم مثالي ، يمكن أن يتكون هذا المزيج المحتمل من مزيج من عقارين من شأنه أن يغلق مرور فيروس نقص المناعة البشرية في المستقبلين المشاركين. لأول مرة ، Maraviroc موجود بالفعل ، على الرغم من أن هذه البلورة ستسمح على الأرجح بتطوير عقاقير جديدة تهدف إلى منع استخدام مصحح CCR5 بواسطة فيروس نقص المناعة البشرية. بالنسبة لمستقبلات CXCR4 المشتركة ، لم يكن من الممكن توليد أي دواء ، على الرغم من أن البلورة تم نشرها لمدة ثلاث سنوات. "فشلت جميع المحاولات بسبب سمية" ، يخلص Alcami.
المصدر:



















---waciwoci-i-wartoci-odywcze-ile-kalorii-ma-kiwi.jpg)





